|
|
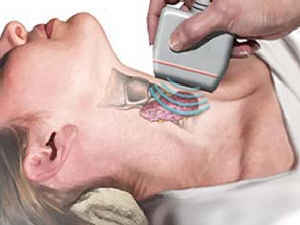
50% מהחולים בארה"ב יושפעו [צילום: National Institue of Health U.S.A]
|
|
|
|
|
חברת אנטרה (ביו), שהגישה לפני כשלושה חודשים בקשה להכרה בתרופה האוראלית שלה לטיפול בתת פעילות בלוטת יותרת התריס (Hypo-Parathyroidisim), קיבלה ממנהל המזון והתרופות בארה"ב (FDA) אישור להכרה במעמד של התרופה כתרופת יתום.
די.אן.איי ביומדיקל מחזיקה בכ-52% מהונה המונפק והנפרע, בדילול מלא, של אנטרה.
בלוטות יותרת התריס הן 4 בלוטות הממוקמות בצמוד לבלוטת התריס אחראיות על וויסות רמת הסידן בגוף. בעת מחסור בסידן מפרישות הבלוטות הורמון בשם PTH (Parathyroid Hormone) הגורם לעליה ברמת הסידן. תת-פעילות בבלוטות נוצרת במקרים בו הן נפגעו או הוצאו בניתוח לכריתת בלוטת התריס או מחוסר תפקוד הנובע מניוון או מסיבות שונות. הטיפול המקובל כיום לטיפול במחלה ניתן באמצעות לקיחת סידן וויטמין D ותרופות אחרות לטיפול בסימפטומים של המחלה. מאחר שברוב המקרים נדרש החולה לקחת כמויות יחסית גדולות של סידן, נוצרות תופעות לוואי בעיתיות כגון הפרעות נוירולוגיות, אבנים בכליות, וכולי.
בהמשך להודעת החברה בעבר כי החומר הפעיל המשמש לתרופה האוראלית שהיא מפתחת כיום לטיפול באוסטאופורוזיס, הורמון ה-PTH, יכול לשמש גם כתרופה יעילה למחלת תת-פעילות בלוטת יותרת התריס.
החברה הודיעה באוגוסט 2013 על כוונתה לבצע ניסויים קלינים בבני אדם במרכז רפואי באנגליה, אשר אמור להתבצע ב 10-15 מתנדבים החולים במחלה ובמשך תקופה של 4 חודשים.
על-פי הידוע, היקף המחלה בארה"ב מוערך בכ-50,000 חולים בארה"ב בלבד. החברה מעריכה כי התרופה שהיא מפתחת תתאים לכ-50% מהם. אנטרה הדגישה כי הינה ממשיכה במקביל בפעילות הפיתוח של התרופה האוראלית לטיפול באוסטאופורוזיס.
סטטוס תרופת יתום קיים בארה"ב מאז שנת 1983 והוא מוסדר בחוק. הוא נועד לתת תמריץ לפיתוח תרופות בעלות פוטנציאל למנוע או לטפל במחלות קשות אשר משפיעות על פחות מ-200,000 אנשים בארה"ב. הסיווג כתרופת יתום הוא בעל השפעות נרחבות מבחינה רגולטורית ומסחרית והוא מקנה, בין היתר, שבע שנות בלעדיות בשוק לאחר אישור התרופה לשיווק (ללא קשר למעמד הפטנט), קיצורי לוחות זמנים, הנחה בעלויות של המשך ההליך הרגולטורי מול ה-FDA, זיכויי מס משמעותיים ועוד.